Tuberculosis: el gran maestro del engaño inmunológico
Hilda Cecilia Leyva Sánchez, Leonor Pérez Martínez y Martin Gustavo Pedraza Alva
¿Cómo logra una bacteria tan antigua como Mycobacterium tuberculosis (Mtb) convertir a nuestras propias células defensoras en cómplices para su supervivencia? Este microorganismo, causante de la tuberculosis (TB) (Figura 1), es difícil de eliminar porque se refugia dentro de los macrófagos, que son células encargadas de ingerir y destruir patógenos, y altera las señales inflamatorias, esos mensajes que las células envían cuando hay una infección, debilitando así nuestras defensas. En este duelo microscópico lleno de estrategia: ¿ganará nuestro cuerpo o la infección?

Figura 1. Síntomas de la tuberculosis.
¿Cómo afecta la tuberculosis a nuestro cuerpo?
Al inhalar gotitas cargadas de Mtb, la bacteria llega a los pulmones (Figura 2) e infecta a los “macrófagos alveolares”, los "guardianes" del sistema respiratorio. Normalmente, estos destruirían a la bacteria en compartimentos llamados “fagolisosomas” (Figura 3), que funcionan como un triturador celular, algo así como el estómago del macrófago. Sin embargo, Mtb es un maestro del engaño; en lugar de ser destruido, manipula a los macrófagos para convertirlos en su refugio, usando “receptores celulares” que son como “antenas” que están en su superficie y le ayudan a detectar señales para evitar su eliminación.
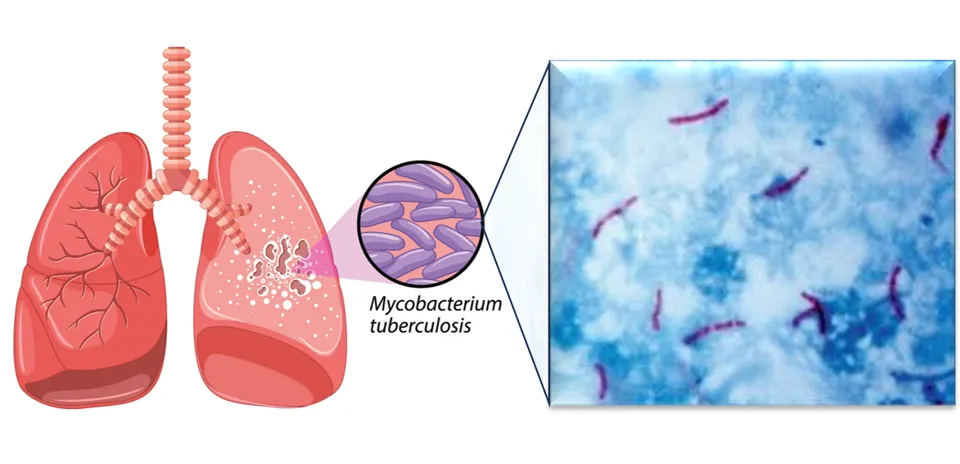
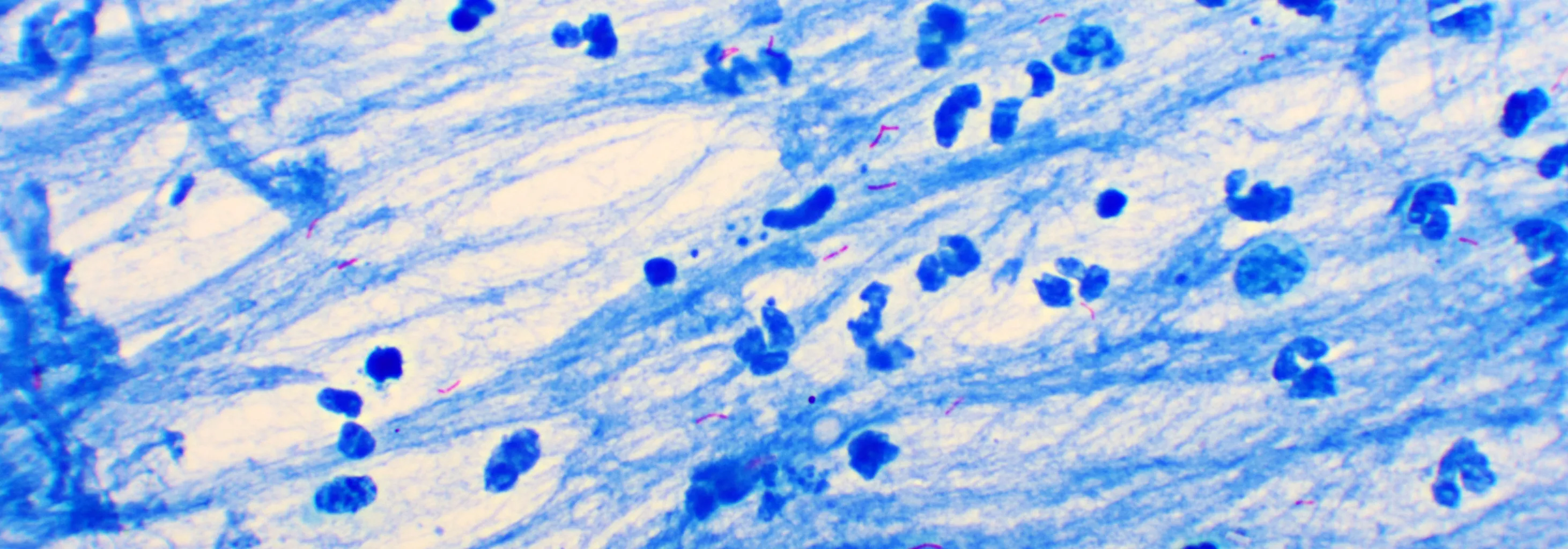
Figura 2. Imagen microscópica de Mycobacterium tuberculosis, teñida con la técnica de Ziehl-Neelsen que permite identificar a estas bacterias.
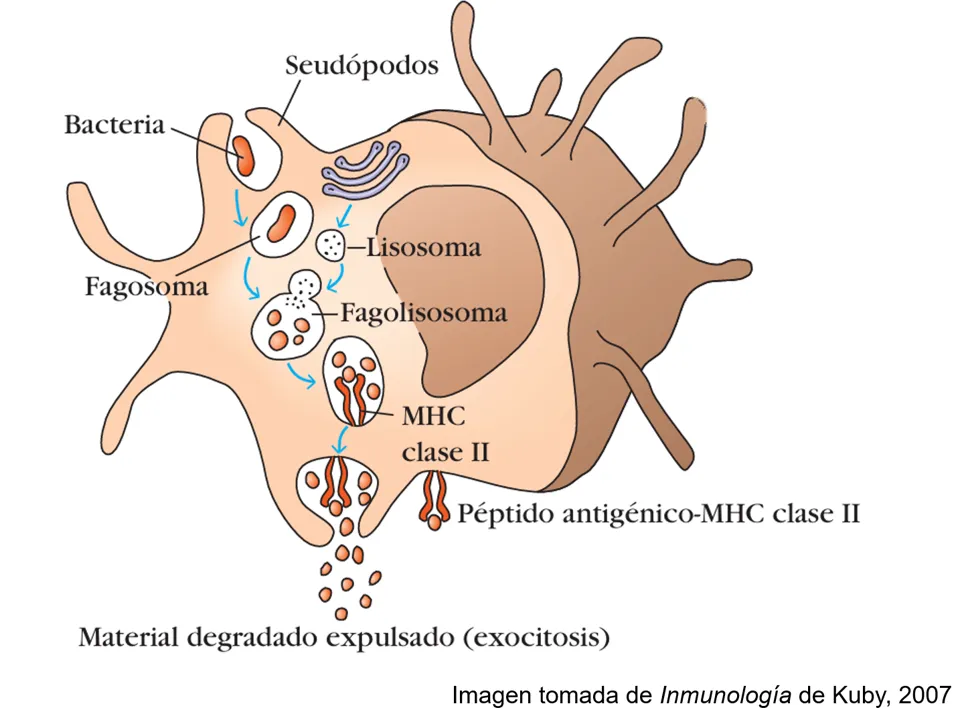
Figura 3. En la fagocitosis, la célula engloba a la bacteria con seudópodos, formando un fagosoma que se fusiona con lisosomas para crear el fagolisosoma. La bacteria se degrada y sus fragmentos se colocan en la superficie de la célula usando proteínas especiales (como el complejo mayor de histocompatibilidad (MHC) clase II), para mostrarlos a otras células del sistema inmunológico, como los linfocitos T, y así activar una respuesta más específica. El material que no se necesita, es expulsado fuera de la célula.
Un delicado equilibrio de citocinas
Cuando Mtb infecta el cuerpo, activa unas señales químicas llamadas “citocinas”, que funcionan como mensajeros del sistema inmunológico. Al inicio de la infección, el sistema inmune envía "mensajes de alerta" a través de las llamadas “citocinas proinflamatorias” pequeñas señales químicas que avisan sobre la infección y que tienen nombres complicados, como TNF (factor de necrosis tumoral), IL-1β e IL-6, que ayudan a controlar la replicación bacteriana y son esenciales para atraer otras células inmunitarias como las que se llaman neutrófilos, células dendríticas y células NK (Figura 4) que ayudan a detectar la infección, atacar al invasor y coordinar una respuesta más completa del sistema inmunológico. Pero Mtb ha desarrollado una interesante estrategia. Después de un tiempo, logra que el cuerpo produzca citocinas antiinflamatorias, como las que se llaman IL-10 y TGF-β, que funcionan como un "control" que reduce o suprime la respuesta de las defensas. Es como si la bacteria “engañara” al sistema inmune para que deje de atacarla, permitiéndole quedarse y multiplicarse sin problemas.
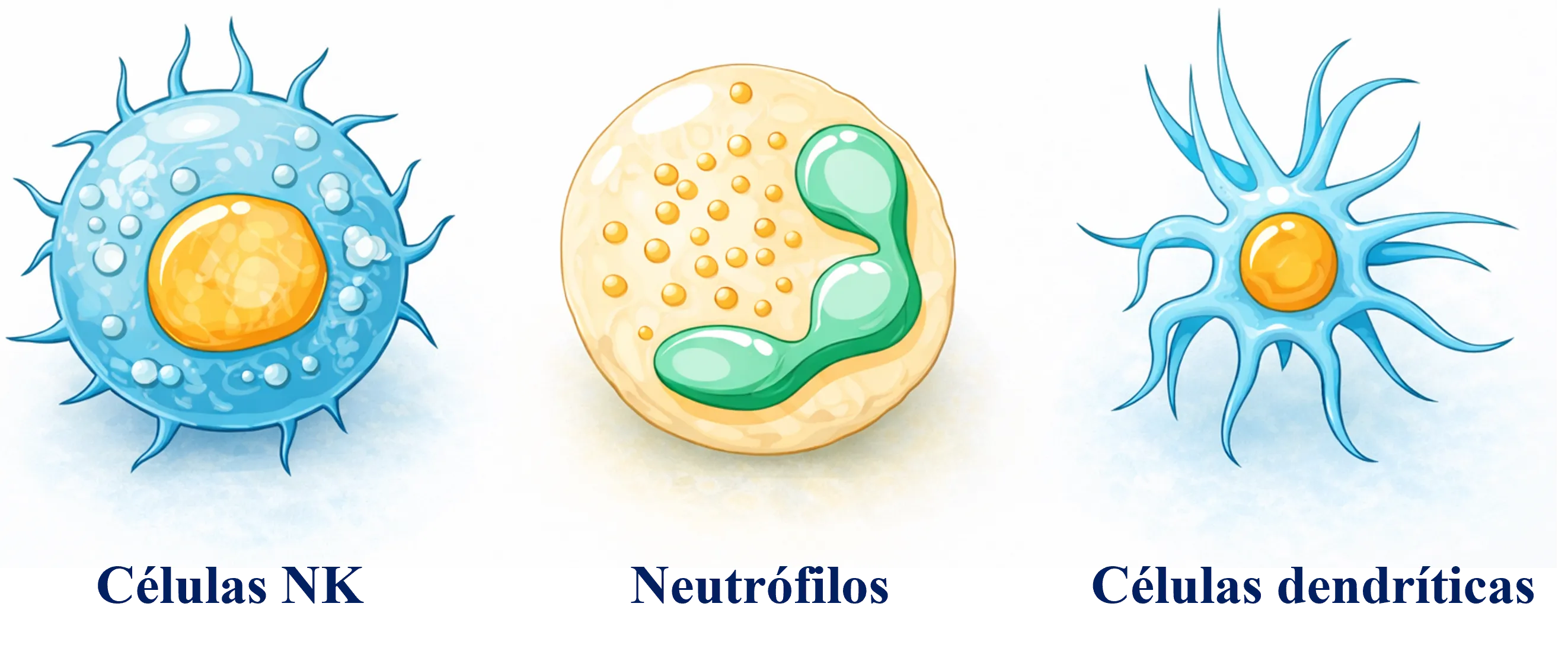
Figura 4. Tres aliados clave de tu sistema inmune. Las células NK eliminan células dañinas, los neutrófilos combaten infecciones de forma inmediata y las células dendríticas ayudan a “avisar” al resto del sistema inmune para montar una defensa más específica.
El éxito de la tuberculosis como enfermedad reside en un frágil equilibrio entre las moléculas que estimulan y las que suprimen la inflamación, que es una respuesta de defensa del cuerpo cuando hay una infección, una herida o algún daño y que algunas veces puede causar —como efecto visible— la hinchazón. Este equilibrio puede definir el destino del huésped: eliminar la bacteria o formar granulomas (estructuras que son como murallas de células que intentan encerrar a la bacteria, aunque sin lograr destruirla) (Figura 5).
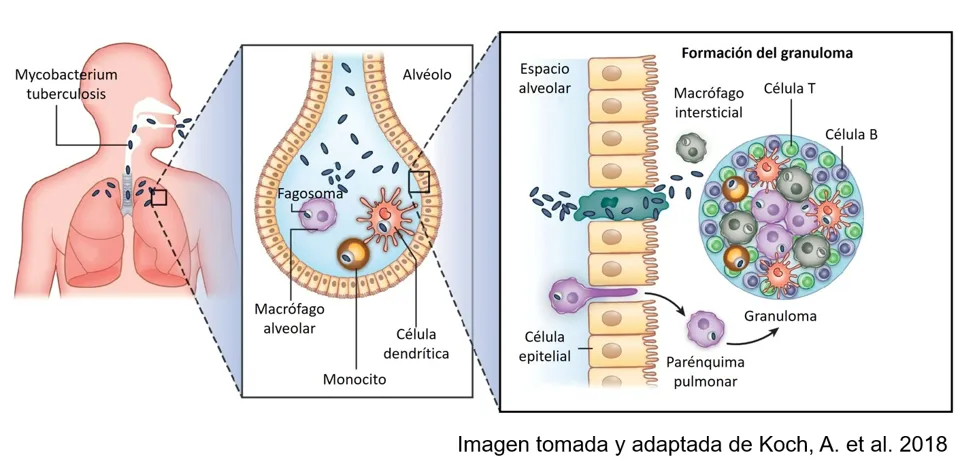
Figura 5. Ingreso de Mycobacterium tuberculosis a los pulmones y respuesta del sistema inmune con la formación de granulomas, estructuras celulares que intentan contener la infección.
Una molécula importante: el interferón gamma
El interferón gamma (IFNγ) es una molécula clave en la lucha contra Mtb. Su papel en el control de la enfermedad durante las fases tardías de la infección, específicamente en la formación y mantenimiento de los granulomas, ha sido demostrado por numerosos estudios tanto en modelos animales como en pacientes con TB.
Esta citocina estimula a las células encargadas de ingerir y destruir bacterias, aumentando su capacidad para eliminarlas. A pesar de esto, en algunos casos, niveles elevados de citocinas antiinflamatorias como IL-10 contrarrestan los efectos del interferón (IFNγ), lo que permite que la enfermedad progrese. Sin embargo, esta molécula también puede desempeñar un papel crucial en las etapas tempranas de la infección. Cuando Mtb entra en contacto con los macrófagos alveolares en los pulmones, éstos producen esta importante señal que los ayuda a destruir a la bacteria, ya que promueve un proceso que también tiene un nombre difícil de leer: “macropinocitosis”, una especie de "trampa" que las células inmunitarias utilizan de manera alternativa a la fagocitosis para comerse y eliminar a los invasores (Figura 6).
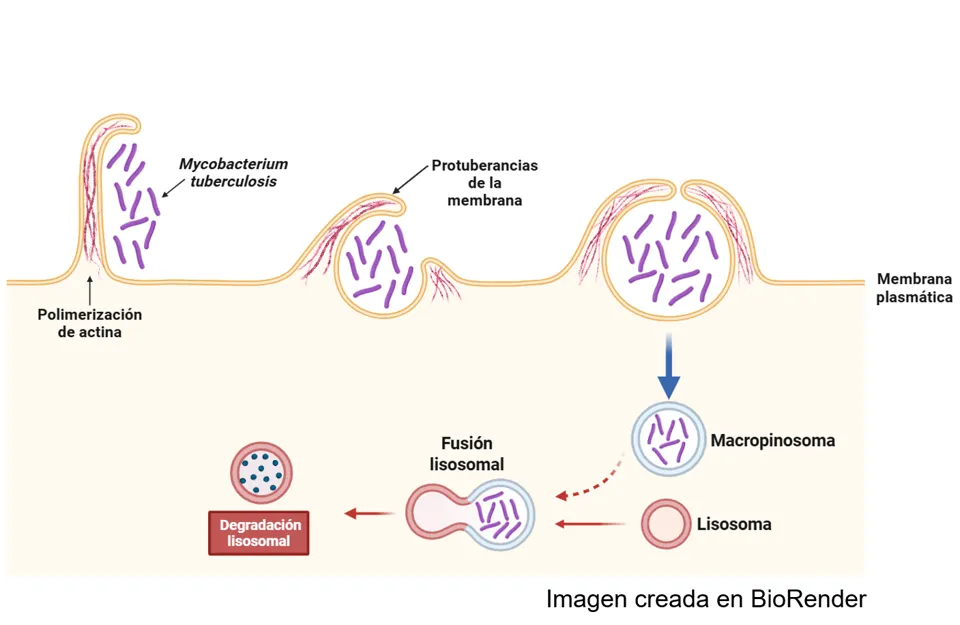
Figura 6. Proceso de entrada de Mycobacterium tuberculosis en la célula mediante “macropinocitosis”, un mecanismo que mejora la captación bacteriana y la actividad bactericida de la célula huésped.
¿Podremos usar el propio sistema inmunológico para vencer a esta bacteria?
Investigaciones recientes han revelado el papel crucial de una molécula que se llama “KLF10”, un factor de transcripción que es como un "director de orquesta" de la célula, ya que decide qué genes se deben encender o apagar para producir diferentes proteínas, de esta manera regula la expresión (producción) tanto de las citocinas proinflamatorias como de las antiinflamatorias. En condiciones normales, KLF10 mantiene un equilibrio entre los distintos tipos de citocinas, controlando la inflamación. Sin embargo, durante la infección por Mtb, KLF10 es influenciado para favorecer un ambiente antiinflamatorio, es decir, un conjunto de señales que disminuyen la respuesta inflamatoria y, de esta manera, facilitan la supervivencia de la bacteria (Figura 7).
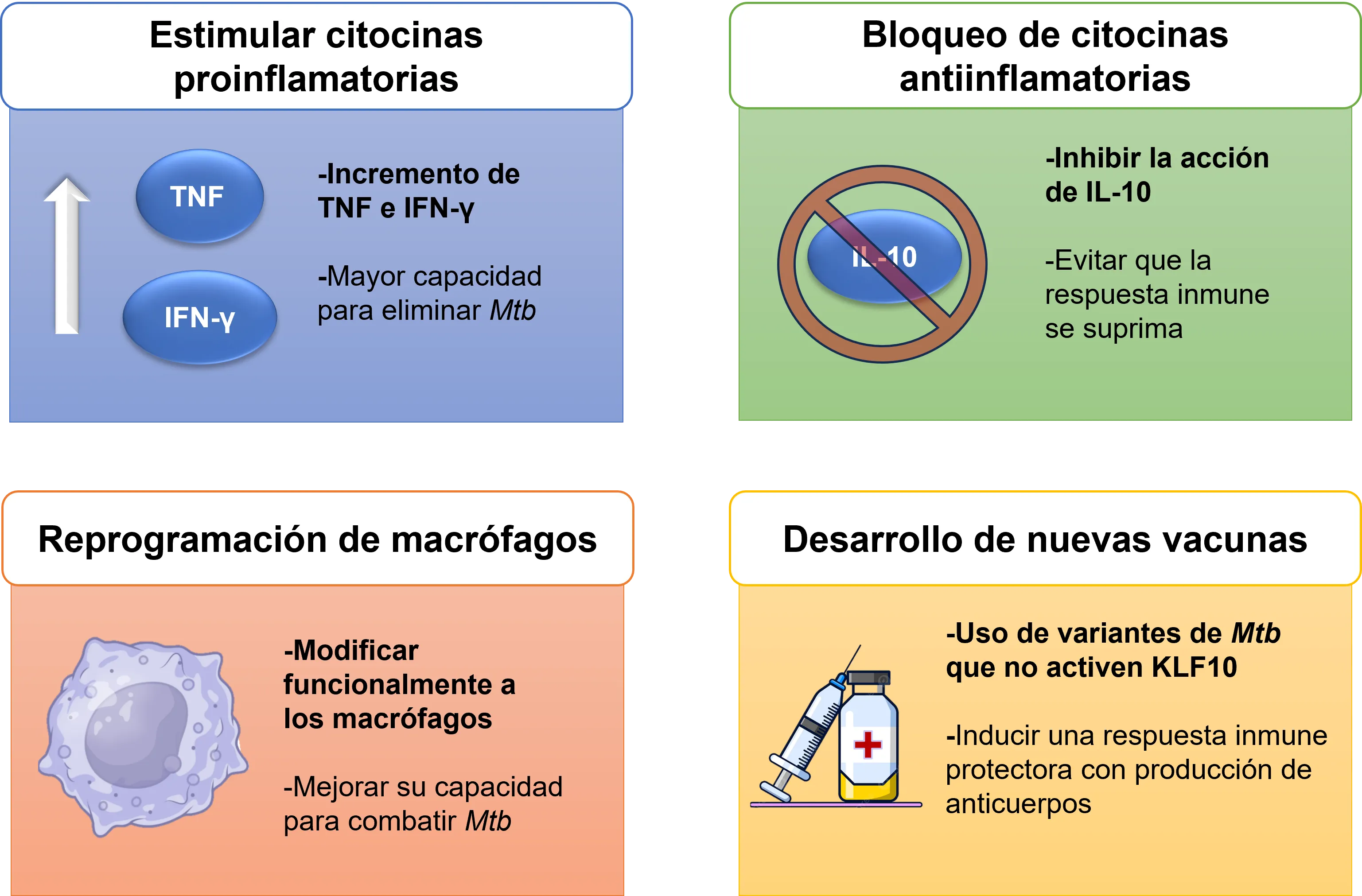
Figura 7. Papel de KLF10 en la regulación de la respuesta inmunológica frente a Mycobacterium tuberculosis. La ausencia de KLF10 (KLF10 KO) promueve un ambiente proinflamatorio, es decir, promueve que el sistema inmunológico esté más activo y, a su vez, favorece la macropinocitosis, favoreciendo la destrucción de Mtb. Por el contrario, su presencia induce un ambiente antiinflamatorio permitiendo la supervivencia de la bacteria. Imagen creada en BioRender.
En nuestro grupo hemos demostrado que, cuando los macrófagos carecen de KLF10, producen más citocinas inflamatorias (incluido el interferón IFNγ), haciéndolos más eficaces para destruir a Mtb (Figura 7). Esto abre la posibilidad de explorar nuevas terapias que modulen la acción de KLF10, con el fin de mejorar el control de la enfermedad (Figura 8).
La tuberculosis no es solo una batalla entre una bacteria y el cuerpo, sino un juego estratégico, donde ambas partes intentan ganar ventaja. Aunque Mtb tiene estrategias impresionantes para evadir las defensas de nuestro cuerpo, la ciencia está desentrañando estos secretos para diseñar terapias más efectivas. Al final, el objetivo es claro: ayudar a nuestro sistema inmunológico a ganar esta batalla y reducir el impacto de la enfermedad en el mundo.
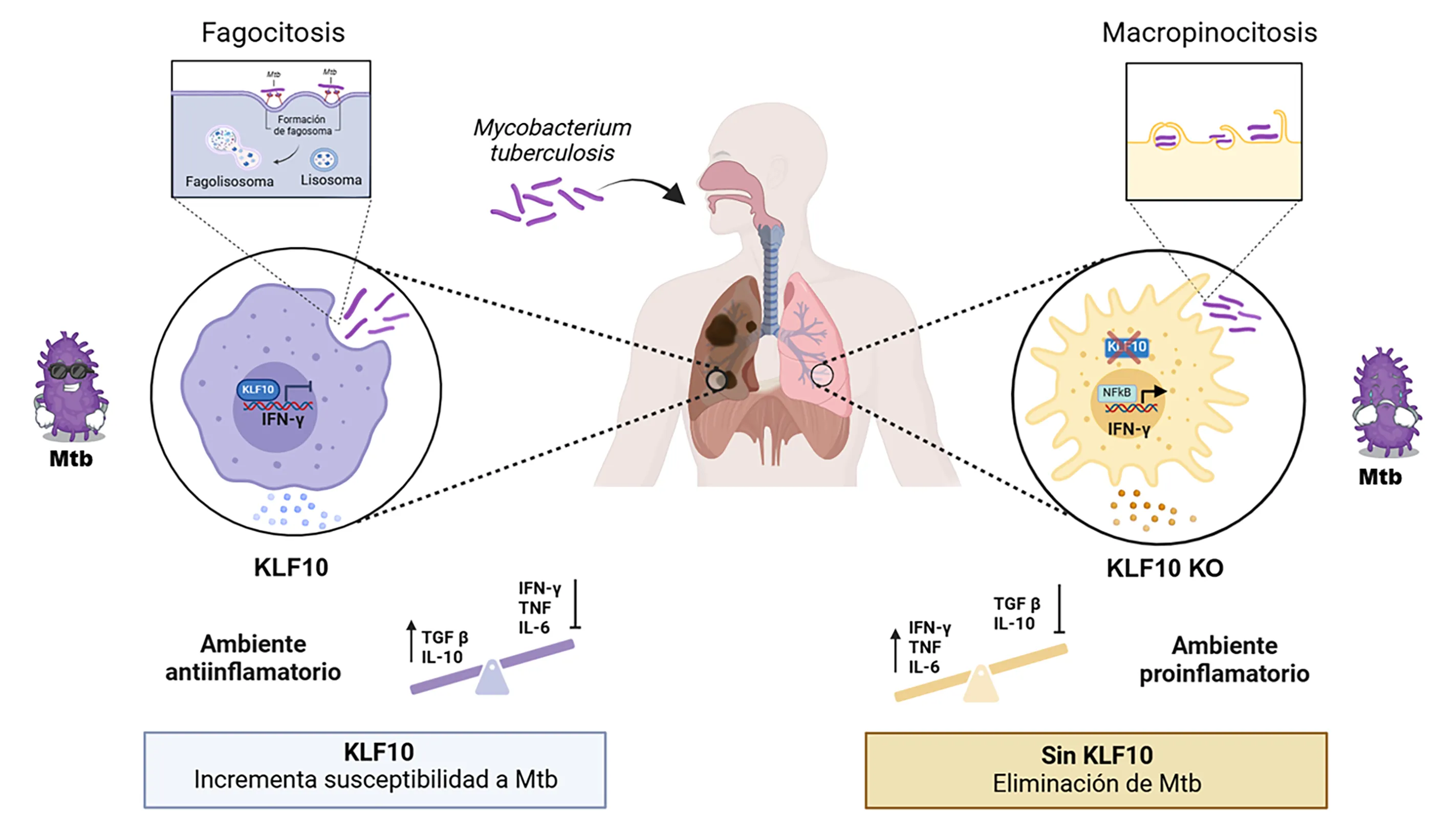
Figura 8. Terapias innovadoras contra la tuberculosis que van más allá del uso de antibióticos convencionales.
Lecturas recomendadas
- Araujo Z, et al. “Respuesta inmunitaria en tuberculosis y el papel de los antígenos de secreción de Mycobacterium tuberculosis en la protección, patología y diagnóstico: Revisión. Investigación Clínica” (2008). http://ve.scielo.org/scielo.php?script=sci_arttext&pid=S0535-51332008000300012&lng=es&tlng=es.
- Peregrino, E. S., Castañeda-Casimiro, J., & Wong-Baeza, I. (2024). Tuberculosis: Una sombra del pasado que sigue vigente a través del tiempo. Revista El Linfocito (4). https://sociedadmexicanadeinmunologia.org/wp-content/uploads/2024/03/01_Tuberculosis-El-infocito-No4-Mzo-2024.pdf
- Flores Valdez, M.A. (2016). Generación de candidatos a vacunas contra tuberculosis en México. Biotecnología en Movimiento, 4, 25-26. Instituto de Biotecnología de la UNAM. https://biotecmov.ibt.unam.mx/services/pdfDownloader.php?id=NCoqXyoqMTI=
- Alemán Navarro, E., & Rosenstein Azoulay, Y. (2024). Pero... ¿la tuberculosis, no estaba ya erradicada? Biotecnología en Movimiento, 36, 36-1. Instituto de Biotecnología de la UNAM. https://biotecmov.ibt.unam.mx/numeros/36/1.html
- Flores Valdez, M.A. (2024). Regreso al pasado, pero ¿con ventajas? La vacunación contra tuberculosis vía intravenosa. Biotecnología en Movimiento, 36, 36-6. Instituto de Biotecnología de la UNAM. https://biotecmov.ibt.unam.mx/numeros/36/6.html
Comparte este artículo en redes sociales

Acerca de los autores
La Dra. Leonor Pérez Martínez es Investigadora Titular ¨C¨ de Tiempo Completo en el Departamento de Medicina Molecular y Bioprocesos del Instituto de Biotecnología-UNAM, donde dirige el grupo de Neuroinmunobiología. Es bióloga por la UNAM y realizó estudios de posgrado en el Instituto Weizmann de Ciencias (Israel) y en el Instituto Friedrich Miescher (Suiza), además de una estancia posdoctoral en la Universidad de Vermont, EUA. Su investigación se enfoca en los mecanismos moleculares de la inflamación y su relación con el envejecimiento y enfermedades crónico-degenerativas como el Alzheimer, así como en el papel de los microRNAs en la salud y enfermedad. Ha liderado diversos proyectos científicos, publicado numerosos trabajos y formado recursos humanos en distintos niveles académicos. Asimismo, participa activamente en divulgación científica y en iniciativas de investigación interdisciplinaria. El Dr. Martín Gustavo Pedraza Alva es Investigador Titular "C" de Tiempo Completo en el Departamento de Medicina Molecular y Bioprocesos del Instituto de Biotecnología de la UNAM, donde dirige el grupo de Neuroinmunobiología. Es biólogo por la UNAM, con estudios de posgrado en el Instituto Weizmann de Ciencias (Israel) y doctorado en Bioquímica por el Instituto Friedrich Miescher (Suiza). Su labor científica se centra en el estudio molecular de la comunicación neuro-inmune, la interacción hospedero-patógeno y el papel de la inflamación en diversas enfermedades. A través de herramientas de biología molecular e inmunología, busca comprender cómo se regulan las respuestas inflamatorias y su impacto en padecimientos infecciosos y crónico-degenerativos. Ha publicado numerosos artículos y participa activamente en la formación de recursos humanos, la divulgación científica y el desarrollo de proyectos de investigación. La Dra. Hilda Cecilia Leyva Sánchez es Investigadora Posdoctoral SECIHTI en el grupo de Neuroinmunobiología dentro del Departamento de Medicina Molecular y Bioprocesos del Instituto de Biotecnología de la UNAM. Obtuvo su Maestría y Doctorado en la Universidad de Guanajuato, donde investigó los mecanismos de regulación genética involucrados en la mutagénesis adaptativa en Bacillus subtilis. Actualmente, su trabajo se enfoca en comprender cómo el sistema inmunológico responde a Mycobacterium tuberculosis y cómo distintos reguladores genéticos influyen en la respuesta inflamatoria y en el control de la infección. Asimismo, participa activamente en actividades de divulgación científica.
Contacto: leonor.perez@ibt.unam.mx; gustavo.pedraza@ibt.unam.mx; hilda.leyva@ibt.unam.mx